血糖のホメオスタシスで忘れがちなもう一つの視点—その1
加藤 潔 記
紹介論文
メトフォルミン血糖値低下作用の第一次作用点は腸管であり、循環系ではない。
The primary glucose-lowering effect of metformin residues in the gut, not in the circulation: Results from short-term pharmacokinetic and 12-week dose-ranging studies. Diabetes Care 2016; 39:198-205
John B. Buse, Ralph A. DeFronzo, Julio Rosenstock, Terri Kim, Colleen Burns, Sharon Skare, Alain Baron, and Mark Fineman
(Corresponding author: Fineman, M, Elcelyx Therapeutics, San Diego, CA)
通常の即溶解性メトフォルミン(Met IR)を小腸下部(pH6.5)まで溶解を遅らせる外皮で覆った遅溶解性メトフォルミン錠(Met DR)を用い、Metを下部小腸(主に回腸)で作用させることで起こる血糖の降下を即溶解性(immediate type IRとextended type XR)メトフォルミン錠のそれと比較して、Metにより血糖降下が誘起される機構についての新たな可能性を提示した。
論文の概要
Metが2型糖尿病(T2DM)の経口治療薬として導入されて以来50年以上経過し、1990年代以降は最初に投与すべき経口治療薬として定着している。しかし、その血糖値低下の作用機作については諸説がある。Metの作用として、(a) 肝臓のLKB1を介したAMPKsの活性化、(b) グルカゴンが活性化するcAMP 合成の阻害、(c)ミトコンドリア内膜上の電子伝達複合体Iを阻害してATP生成を抑制することで細胞のエネルギー充足率を下げる(AMP/ATP比が増大)、(d) 解糖により細胞質で生成する還元型補酵素(NADH)をミトコンドリア内に運び込んでATPの生成にあてるためのシャトル(搬入)酵素を阻害して細胞質内NADH濃度を上昇させると糖新生(乳酸、グリセリンからブドウ糖が生成)が阻害されること(同時にFADを介する電子伝達が抑制されてATPの生産も減少する)、などが報告されている。しかし、 Metによる血糖低下作用にいずれの過程の寄与が大きいかについては判っていなかった。
薬理学の常識からするとMetの臨床投与用量は極めて多く(一錠250mgのMet錠剤を一日に2~8錠服用する)、静注によるMet投与の血糖低下効果は腸管経由に比べると有意に劣る。そこで著者らは、即溶解性Met IR (immediate release)及び XR (extended release)錠と遅溶解性のMet DR (delayed release)錠について、服用後のMetの薬理速度論的および12週の用量範囲試験解析を行った。
研究は、(1) 健常者(20人)を対象とする服用Metの利用効率、(2) 糖尿病患者(240人)を対象とした即溶解性、遅溶解性Met錠によるMetの血糖低下効果の用量-応答特性(dose response)と血中乳酸生成量についての比較検討をした。
研究 1(健常者).:
(1) 血中Met濃度の時間経過:1000 mgを一日2回に分け(12時間空ける)服用すると、即溶Met IRでは血中濃度は服用後すぐ上昇して6時間後に第一のピークが現れるが、遅溶Met DRでは~5時間後頃から緩やかに上昇して11時間後により低いピーク濃度(IRのおよそ70%)に達する。第二のピークは、IRでは15時間後で濃度は第一ピークより10% 程高いが、DRでは19時間後で濃度は第一ピークの71%と低くなった。両者ともに28時間後には服用前の濃度に戻った。
(2) Met DR 1000mg、500mgのMetの有効利用量は1000 mg Met IRに比べてそれぞれ52%、68%少なく、2000 mg Met XRに比べると48%、65%少ない。
研究 2(糖尿病患者).:
(1) Met錠の血糖低下効果:
Met錠4週間処理の血糖低下効果の用量応答性(dose response)
| 一日の服用量 | 偽薬 | Met DR | Met XR |
|---|---|---|---|
| 600 mg | -4 mg/dL | -11 mg/dL | |
| 800 mg | -13 mg/dL | ||
| 1000 mg | -18 mg/dL | -12 mg/dL | |
| 2000 mg | -25 mg/dL |
DR Metの有効利用量はXRに比べて少ないにも拘わらず、血糖降下作用は実効的にはMet DR (600 mg) ≃Met XR (1000 mg)であり、 12週後のHbA1cの変化もこれに矛盾しない。ちなみに、利用されなかったMet は糞便と共に排出される。
(2) 循環血のMet濃度: Met DRでは循環血のMet濃度は臨床服用量に関係無く〜100 ng/mLとほぼ一定であるが、 Met XRでは1000 mg, 2000 mgでそれぞれ ~500 ng /mL , ~800 ng /mLと明らかな用量-応答性がみられ、且つその濃度はDRより数倍以上高かった。 Met DR (1000 mg)服用時の循環血Met濃度はMet XR 1000 mgの~20%、2000 mgの~10%と低い(Fig 2C)。
(3) 血中乳酸量: Met服用開始後12週の空腹時血中乳酸濃度はXRで約2倍(0.33 mmol/L)に増加するが、DRでは偽薬レベル(0.16 mmol/L)に留まる。従って、DRの服用による乳酸アシドーシス発生の危険度はXRに比べるとかなり低下するものと推定される。
(4) Met DRで最も多い副作用は胃腸障害であるが、即溶解剤MetであるGlucophage錠の添付注意書に記されているレベル内におさまる。
結論:Met(メトフォルミン)は2型糖尿病経口治療薬の第一選択肢として広く使用されている。Metは陽イオン輸送体OCT1を介して先ず腸管壁上皮粘膜細胞に取り込まれ蓄積
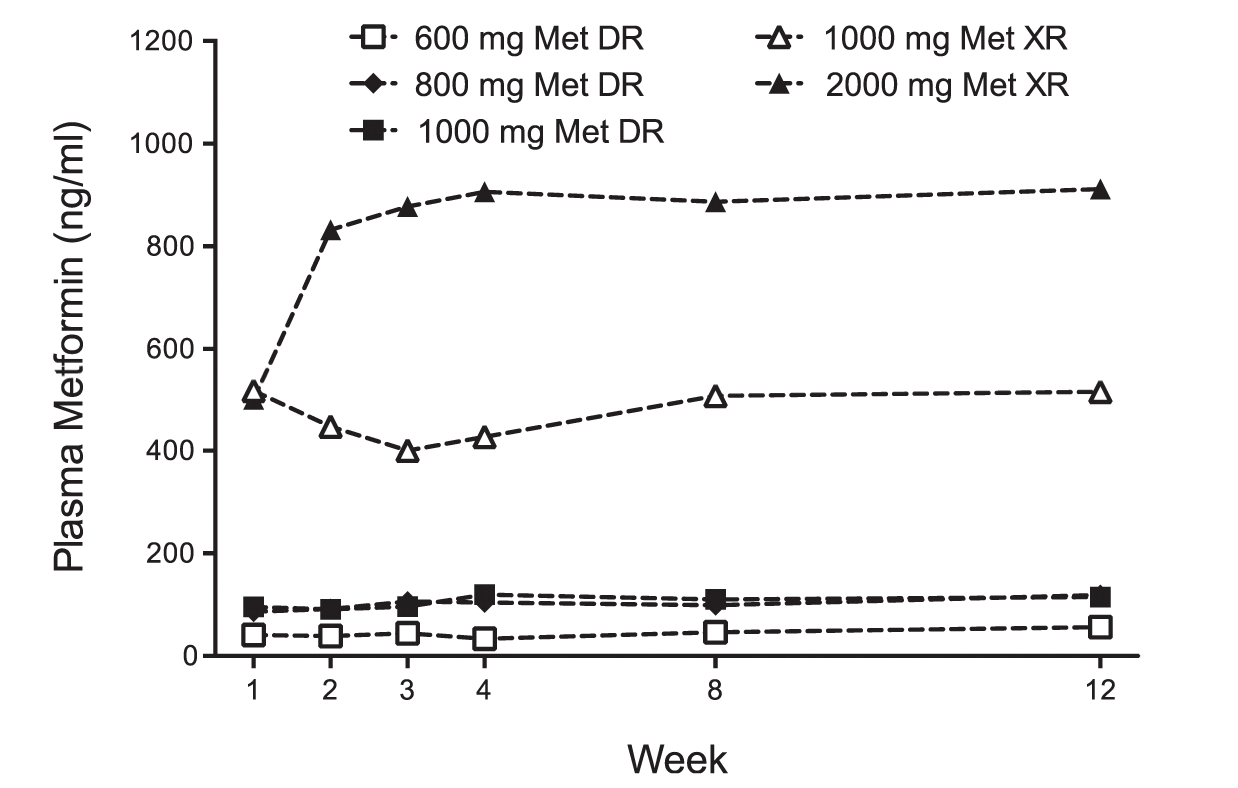
空腹時血中Met濃度 (中央値) Fig 2Cより
されるが、次いで漿膜側から循環血中へ分泌されて血流に乗り体内を巡る。標的器官である肝臓、腎臓に達して臓器細胞に取り込まれて細胞の糖代謝に影響するが、最終的には自身は代謝されずに腎臓で尿中へ排出され体外に放出される。Metは肝臓における糖新生を抑制するので、その肝臓の代謝系に及ぼす影響が注目されてきた。しかし、Metの肝細胞内濃度は血中濃度の~10倍に上がるものの、小腸管壁細胞内では血中濃度の300倍にも達する上、MetがGLP-1など胃腸ホルモンの分泌を促進するとの報告もある。
これらを踏まえ著者らは、血糖降下反応に繋がるMetの腸管への主要作用部位が従来考えられていた上部小腸(十二指腸、空腸)だけでなく下部小腸(回腸)の細胞に及ぶ可能性を検討した。
Metが血中GLP-1を増加させるとの報告は以前から議論になっていたが、GLP-1の血中濃度上昇にMetとDPP-4 阻害剤とが加算効果を示すとの報告(Migoya et al. 2010)があり、インクレチンを分泌するL-細胞の分布密度が回腸管腔壁で高いことから、MetによるL-細胞のインクレチン分泌促進が血糖の主要な低下作用であると考え、Metの血糖低下効果の70%は回腸経由であると見積もった。
この結論は、血中の高濃度Metが肝臓で(NADHのミトコンドリア搬入を阻害して)乳酸とグリセロールのグルコース変換(糖新生)を抑制するとの報告(Madiraju et al. 2014)と矛盾しない。血中の高濃度のビグアナイド剤は乳酸経由の糖新生を阻害するので乳酸の血中濃度が上がり乳酸アシドーシのスリスクが高まるが、遅溶解性Met DRは血中Metの濃度の上昇を低く抑えるため、乳酸の血中濃度は偽薬レベルに留まる。これによりMetの適用範囲が従来より広がる可能性が開ける。





